表觀遺傳 | STTT:南(nán)京醫科大(dà)學張業偉團隊通(tōng)過工程細胞外囊泡用(yòng)于癌症相關成纖維細胞的(de)靶向重編程,以增強胰腺癌的(de)治療
胰腺癌是緻命的(de)惡性腫瘤之一,死亡率很高(gāo),目前幾乎沒有治療選擇。胰腺癌中的(de)腫瘤微環境(TME)以纖維化(huà)和(hé)癌症相關成纖維細胞(CAF)的(de)存在爲特征,對(duì)腫瘤進展和(hé)治療耐藥性均起著(zhe)關鍵作用(yòng)。工程化(huà)細胞外囊泡(EV)領域的(de)最新進展爲胰腺癌的(de)靶向治療提供了(le)新的(de)途徑。
2024年6月(yuè)24日,南(nán)京醫科大(dà)學張業偉團隊在Signal Transduction and Targeted Therapy發表題爲“Engineered extracellular vesicles for targeted reprogramming of cancer-associated fibroblasts to potentiate therapy of pancreatic cancer”的(de)研究論文,本研究旨在開發用(yòng)于靶向重編程CAF和(hé)調節胰腺癌TME的(de)工程 EV。從骨髓間充質幹細胞(BMSC)獲得(de)的(de)EV負載miR-138-5p和(hé)抗纖維化(huà)藥物(wù)吡非尼酮(PFD),并用(yòng)整合素α5靶向肽(稱爲 IEV-PFD/138)進行表面修飾,以重編程CAF并抑制其促腫瘤作用(yòng)。整合素α5靶向肽修飾增強了(le)EV的(de)CAF靶向能力。
miR-138-5p 直接抑制 FERMT2-TGFBR1 複合物(wù)的(de)形成,抑制 TGF-β 信号通(tōng)路激活。此外,miR-138-5p通(tōng)過直接靶向 FERMT2-PYCR1 複合物(wù)抑制脯氨酸介導的(de)膠原合成。miR-138-5p和(hé)PFD在EVs中的(de)組合協同促進了(le)CAF重編程,抑制了(le)CAFs的(de)促癌作用(yòng)。使用(yòng)富含原位基質和(hé)患者來(lái)源的(de)異種移植小鼠模型的(de)臨床前實驗産生了(le)有希望的(de)結果。特别是,IEVs-PFD/138 有效地重編程了(le) CAF 并重塑了(le) TME,從而降低了(le)腫瘤壓力、增強了(le)吉西他(tā)濱灌注、改善了(le)腫瘤缺氧,并提高(gāo)了(le)癌細胞對(duì)化(huà)療的(de)敏感性。因此,本研究中制定的(de)策略可(kě)以改善化(huà)療結果。利用(yòng) IEV-PFD/138 作爲靶向治療劑來(lái)調節 CAF 和(hé) TME,代表了(le)一種很有前途的(de)胰腺癌治療方法。

胰腺癌是一種高(gāo)度侵襲性和(hé)緻命的(de)惡性腫瘤,繼續構成重大(dà)的(de)全球健康挑戰。在所有癌症類型中,它被列爲癌症相關死亡率的(de)第三大(dà)貢獻者。腫瘤生長(cháng)和(hé)治療耐藥性都受到癌細胞與腫瘤微環境(TME)之間錯綜複雜(zá)的(de)關系的(de)影(yǐng)響。在TME中,癌症相關成纖維細胞(CAF)調節胰腺癌發病機制所涉及的(de)過程。因此,CAFs的(de)靶向調節是提高(gāo)胰腺癌治療效果的(de)潛在策略。最近,細胞外囊泡(EVs)在細胞間通(tōng)訊中的(de)作用(yòng)及其潛在的(de)治療應用(yòng)引起了(le)科學界的(de)興趣。EV是細胞釋放的(de)膜結合細胞囊泡,可(kě)以将生物(wù)活性分(fēn)子遞送至受體細胞。EV可(kě)以被設計爲通(tōng)過外源載荷将治療劑運送到目标位點。
據報道,骨髓間充質幹細胞(BMSC)是一組具有多(duō)能性的(de)幹細胞,具有抗腫瘤作用(yòng)和(hé)抗纖維化(huà)特性。BMSCs的(de)臨床前和(hé)臨床效果已被廣泛研究。BMSCs的(de)先進提取技術有助于其在臨床上得(de)到廣泛接受。在腫瘤發展過程中,BMSCs可(kě)以被募集到TME并分(fēn)化(huà)爲CAF。7BMSC 衍生的(de) EV(BMSC-EV)具有EV的(de)固有優勢和(hé)與 BMSC相關的(de)特性,使其成爲胰腺癌中選擇性靶向 CAF 的(de)非常有前途的(de)治療方法。貨物(wù)成分(fēn)的(de)操縱與EV靶向能力的(de)提高(gāo)相結合,将使治療藥物(wù)特異性遞送CAFs,調節其功能并抑制其腫瘤促進作用(yòng)。該策略是一種獨特的(de)方法,可(kě)以破壞CAF和(hé)癌細胞之間的(de)相互串擾,逆轉纖維化(huà)TME,從而改善治療結果。
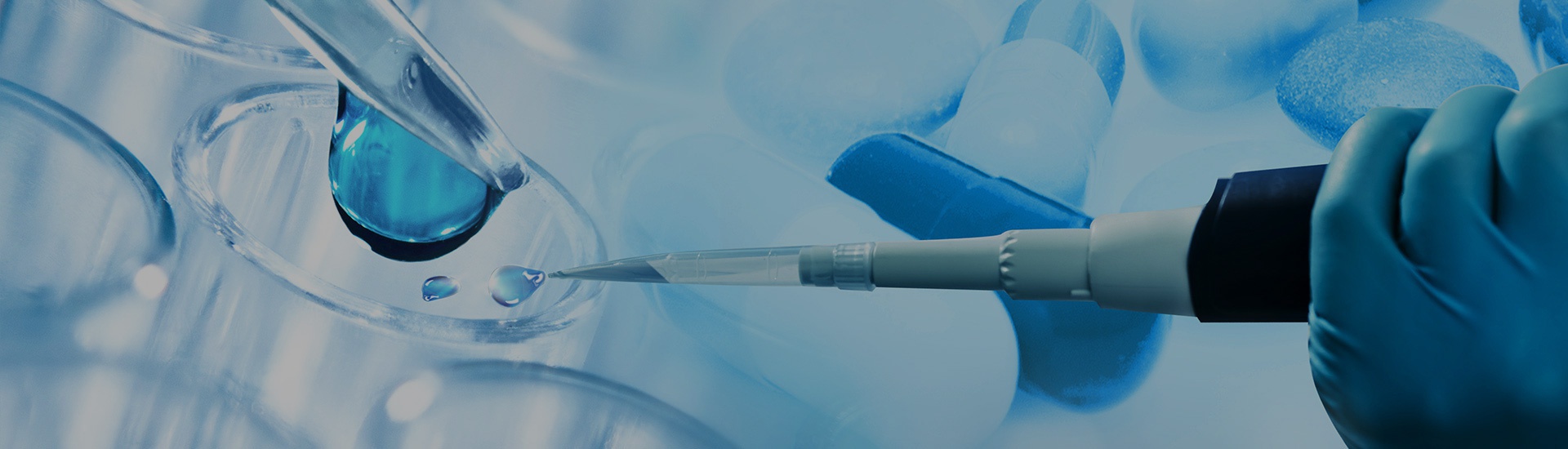
負載miR-138-5p和(hé)吡非尼酮(PFD)并經整合素α5靶向肽(IEVs-PFD/138)表面修飾的(de)細胞外囊泡(EV)的(de)制備和(hé)表征及其增強的(de)癌症相關成纖維細胞(CAF)靶向能力。圖自:Signal Transduction and Targeted Therapy
MicroRNA(miRNA)是一類小的(de)非編碼RNA分(fēn)子,通(tōng)過與mRNA的(de)3'-非翻譯區(qū)(3'-UTR)結合,抑制基因翻譯或下(xià)調靶基因水(shuǐ)平,參與疾病發展的(de)調節。現有文獻表明(míng),miR-138-5p 可(kě)以通(tōng)過利用(yòng)多(duō)種機制抑制癌細胞來(lái)阻止癌症進展。間充質幹細胞(MSC)衍生的(de) EV 中的(de) miR-138-5p可(kě)以靶向SIRT1,抑制人(rén)真皮成纖維細胞的(de)增殖和(hé)遷移,并下(xià)調 NF-κB、α-SMA和(hé)TGF-β1的(de)水(shuǐ)平。然而,之前沒有關于miR-138-5p在CAFs中的(de)功能的(de)研究。一種稱爲吡非尼酮(PFD)的(de)抗纖維化(huà)藥物(wù)用(yòng)于治療特發性肺纖維化(huà)(IPF)。PFD在不同的(de)動物(wù)模型中具有抗炎、抗纖維化(huà)和(hé)抗氧化(huà)功能。此外,在腫瘤治療的(de)背景下(xià),PFD被證明(míng)可(kě)有效抑制TGF-β表達,從而抑制CAF的(de)激活和(hé)膠原蛋白的(de)産生,從而阻礙腫瘤進展。本研究探討(tǎo)了(le)miR-138-5p在胰腺CAFs中的(de)表達和(hé)功能。
接下(xià)來(lái),使用(yòng)超聲處理(lǐ)加載 PFD 和(hé) miR-138-5p的(de) BMSC-EV,并使用(yòng)整合素 α5 靶向肽進行表面修飾,以獲得(de)加載 PFD 和(hé) miR-138-5p的(de)工程整合素 α5靶向EV(IEV)(命名爲 IEV-PFD/138)。采用(yòng)雙熒光(guāng)素酶報告基因和(hé)免疫共沉澱(co-IP)法檢定miR-138-5p的(de)功能機制。采用(yòng)二維(2D)細胞功能實驗、條件培養基(CM)共培養實驗、三維(3D)多(duō)細胞腫瘤球狀體實驗和(hé)皮下(xià)異種移植模型,研究了(le)IEVs-PFD/138對(duì)胰腺CAF靶向重編程的(de)影(yǐng)響。最後,使用(yòng)患者來(lái)源的(de)異種移植物(wù)(PDX)和(hé)富含原位基質的(de)胰腺癌小鼠模型檢查了(le) IEVs-PFD/138 和(hé)吉西他(tā)濱 (GEM)組合的(de)治療效果。